Estuctura fundamental del átomo
¿Cómo se conforma un átomo? ¿Qué relaciones existen entre las partículas que lo componen? ¿Cuáles son las nomenclaturas de sus partes?
Recordemos, primero, que el átomo se define generalmente como la unidad elemental de un cuerpo simple, que conserva las características del elemento a que pertenece, independientemente de las transformaciones químicas.
Los átomos se componen de un núcleo cargado positivamente, de dimensiones sumamente pequeñas, y de una envoltura de electrones cargados negativamente, que se desplazan alrededor del núcleo sobre una o varias órbitas (n).
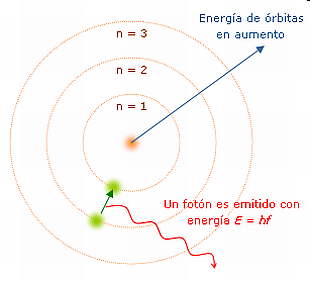 Decimos que el núcleo tiene dimensiones sumamente pequeñas porque, efectivamente, tiene un radio de una cien mil millonésima de centímetro (10^11 mm). Está compuesto, excepto en el caso del hidrógeno, de dos clases de partículas: por una parte, un cierto número de protones y, por otra parte, un cierto número de neutrones, ambos llamados también nucleones.
Decimos que el núcleo tiene dimensiones sumamente pequeñas porque, efectivamente, tiene un radio de una cien mil millonésima de centímetro (10^11 mm). Está compuesto, excepto en el caso del hidrógeno, de dos clases de partículas: por una parte, un cierto número de protones y, por otra parte, un cierto número de neutrones, ambos llamados también nucleones.
Los protones son idénticos al núcleo del átomo de hidrógeno y están cargados positivamente con una carga específica o carga elemental de la misma magnitud (pero de signo contrario) que la del electrón.
Por el contrario, los neutrones son partículas elementales eléctricamente neutras, su masa es prácticamente igual (aunque algo superior) a la de los protones.
Generalmente se utiliza la letra Z para llamar al número de protones, y la N para indicar el número de neutrones del núcleo. La carga positiva de este núcleo comprende, entonces, un número Z de cargas específicas y su masa es aproximadamente igual a Z+N veces la masa de un protón.
 El número de nucleones (neutrones y protones) se simboliza con una A y es lo que constituye el número de masa del átomo.
El número de nucleones (neutrones y protones) se simboliza con una A y es lo que constituye el número de masa del átomo.
La masa del electrón es muy pequeña (1/1836 de la del protón). Su carga ha sido elegida como unidad de carga eléctrica o elemental. Se puede imaginar que los electrones gravitan en órbitas circulares o elípticas alrededor del núcleo, al mismo tiempo que giran sobre sí mismos, como lo hace La Tierra alrededor del Sol.
El movimiento de los electrones de rotación sobre sí mismos se llama spin, o espín. El número de electrones que se pueden encontrar en un átomo está determinado por la energía almacenada en el núcleo (carga) y por las acciones procedentes del exterior, como, por ejemplo, una influencia eléctrica capaz de actuar sobre los átomos.
En los átomos neutros, la carga negativa de los electrones está neutralizada por la carga positiva del núcleo, un átomo de este tipo se dice que no está cargado. Esto implica que el número de los electrones que rodean al núcleo sea igual al número de protones.
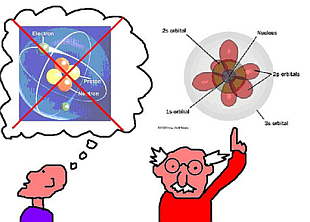 Como primer modelo puede sernos útil imaginarnos los átomos como si se tratase de un sistema planetario, con esferas (electrones) girando alrededor de un centro.
Como primer modelo puede sernos útil imaginarnos los átomos como si se tratase de un sistema planetario, con esferas (electrones) girando alrededor de un centro.
Sin embargo, esto no es más que un modelo precario de lo que hasta ahora se conoce del átomo, que revela ser, en realidad, mucho más complejo que esa representación básica, con orbitales que representan "zonas" en donde los electrones pueden encontrarse.
Así es que los electrones están repartidos en órbitas llamadas capas o niveles electrónicos (que son las capas K, L, M, N, O, P y Q); la capa exterior (o las dos últimas capas) llamadas capa de valencia determina la probabilidad que tiene un átomo de producir ciertas reacciones químicas. La órbita descrita por un electrón en torno a un núcleo atómico no se puede precisar con exactitud.
Fuente: Miriya – espaciociencia.com
