Vacuna experimental contra el Chikungunya podría controlar epidemia en América

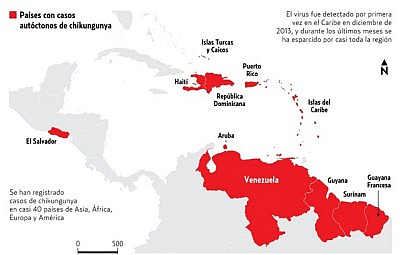
The Lancet, la revista científica británica presenta en su edición de esta semana un artículo titulado Vacuna experimental contra Chikungunya induce una respuesta de anticuerpos vigorosa (Experimental chikungunya vaccine induces robust antibody response). El virus Chikungunya causante de la fiebre del mismo nombre, ha afectado en América a más de 570.000 personas, desde comienzos del año hasta agosto 8.
La vacuna generó anticuerpos neutralizantes (capaces de matar al virus) en todos los 25 voluntarios que se prestaron a participar en el ensayo de desafío realizado por investigadores del Instituto Nacional de Alergía y Enfermedades Infecciosas de EUA (National Institute of Allergy and Infectious Diseases, NIAID), el cual forma parte del NIH.
En el estudio, 23 voluntarios sanos recibieron tres inyecciones (otros dos voluntarios recibieron dos inyecciones) de la vacuna en una de las tres dosis elaboradas (10, 20 o 40 microgramos) en un lapso de 20 semanas. La producción de anticuerpos se midió en varios puntos del tiempo después de cada inyección.
Los investigadores detectaron anticuerpos neutralizantes contra el virus Chikungunya en todos los voluntarios después de la segunda inyección, con un aumento significativo de anticuerpos neutralizantes después de la tercera inyección. Los anticuerpos inducidos por la vacuna persistieron en todos los voluntarios, incluso los que recibieron la dosis más baja, durante al menos 11 meses después de la última vacunación, lo cual sugiere que la vacuna podría proporcionar una protección duradera contra la enfermedad.
Según la investigadora principal del estudio Julie E. Ledgerwood: «La vacuna experimental provocó una respuesta inmunológica fuerte en los individuos receptores con una buena tolerancia» Además destacó que «En particular, las concentraciones de anticuerpos neutralizantes producidos en respuesta a la vacuna fueron comparables a las observadas en los dos pacientes que se había recuperado de la infección por el virus Chikungunya adquirido en otra localidad. Esta observación nos permite ser optimistas respecto a la vacuna, ya que la misma ofrece -por lo menos- la misma protección de la infección natural».
Con información de nih.gov/news y del artículo original
Resumen del Trabajo:
Safety and tolerability of chikungunya virus-like particle vaccine in healthy adults: a phase 1 dose-escalation trial
Chang L-J, Dowd KA, Mendoza FH, Saunders JG, Sitar S, Plummer SH, Yamshchikov G, Sarwar UN, Hu Z, Enama ME, Bailer RT, Koup RA, Schwartz RM, Akahata W, Nabel GJ, Mascola JR, Pierson TC, Graham BS, Ledgerwood JE
Background
Chikungunya virus-a mosquito-borne alphavirus-is endemic in Africa and south and southeast Asia and has recently emerged in the Caribbean. No drugs or vaccines are available for treatment or prevention. We aimed to assess the safety, tolerability, and immunogenicity of a new candidate vaccine.
Methods
VRC 311 was a phase 1, dose-escalation, open-label clinical trial of a virus-like particle (VLP) chikungunya virus vaccine, VRC-CHKVLP059-00-VP, in healthy adults aged 18-50 years who were enrolled at the National Institutes of Health Clinical Center (Bethesda, MD, USA). Participants were assigned to sequential dose level groups to receive vaccinations at 10 ?g, 20 ?g, or 40 ?g on weeks 0, 4, and 20, with follow-up for 44 weeks after enrolment. The primary endpoints were safety and tolerability of the vaccine. Secondary endpoints were chikungunya virus-specific immune responses assessed by ELISA and neutralising antibody assays. This trial is registered with ClinicalTrials.gov, NCT01489358.
Findings
25 participants were enrolled from Dec 12, 2011, to March 22, 2012, into the three dosage groups: 10 µg (n=5), 20 µg (n=10), and 40 µg (n=10). The protocol was completed by all five participants at the 10 µg dose, all ten participants at the 20 µg dose, and eight of ten participants at the 40 µg dose; non-completions were for personal circumstances unrelated to adverse events. 73 vaccinations were administered. All injections were well tolerated, with no serious adverse events reported. Neutralising antibodies were detected in all dose groups after the second vaccination (geometric mean titres of the half maximum inhibitory concentration: 2688 in the 10 µg group, 1775 in the 20 µg group, and 7246 in the 40 µg group), and a significant boost occurred after the third vaccination in all dose groups (10 µg group p=0·0197, 20 µg group p<0·0001, and 40 µg group p<0·0001). 4 weeks after the third vaccination, the geometric mean titres of the half maximum inhibitory concentration were 8745 for the 10 µg group, 4525 for the 20 µg group, and 5390 for the 40 µg group.
Interpretation
The chikungunya VLP vaccine was immunogenic, safe, and well tolerated. This study represents an important step in vaccine development to combat this rapidly emerging pathogen. Further studies should be done in a larger number of participants and in more diverse populations.
Funding
Intramural Research Program of the Vaccine Research Center, National Institute of Allergy and Infectious Diseases, and National Institutes of Health.
Fuente: Felix J. Tapia – felixjtapia.org


